विज्ञान एवं प्रौद्योगिकी
इलेक्ट्रिक बैटरियाँ और इलेक्ट्रोकेमिकल सेल
- 16 Nov 2023
- 11 min read
प्रिलिम्स के लिये:इलेक्ट्रोकेमिकल सेल, इलेक्ट्रिक वाहन, वोल्टाइक सेल, लिथियम-आयन प्रौद्योगिकी, वर्ष 2019 के लिये रसायन विज्ञान में नोबेल पुरस्कार, इलेक्ट्रिक बैटरी के अनुप्रयोग। मेन्स के लिये:इलेक्ट्रोकेमिकल सेल, बैटरियों का विकासवादी प्रक्षेप पथ। |
स्रोत: द हिंदू
चर्चा में क्यों?
इलेक्ट्रिक बैटरियों और इलेक्ट्रोकेमिकल सेल की प्रगति ने परिवहन और ऊर्जा जैसे क्षेत्रों में प्रौद्योगिकी क्रांति लाकर विशेष रूप से ध्यान आकर्षित किया है, जो हमें एक स्थायी भविष्य की ओर ले जाता है।
इलेक्ट्रिक बैटरियाँ और इलेक्ट्रोकेमिकल सेल क्या हैं?
- इलेक्ट्रिक बैटरियाँ :
- इलेक्ट्रिक बैटरी एक ऐसा उपकरण है जो रासायनिक ऊर्जा को संग्रहीत करता है और इसे बिजली में परिवर्तित करता है।
- बैटरियाँ एक या अधिक इलेक्ट्रोकेमिकल कोशिकाओं से बनी होती हैं जो बाहरी इनपुट और आउटपुट से जुड़ी होती हैं।
- इलेक्ट्रिक बैटरियों ने मोटराइज़ेशन और वायरलेस प्रौद्योगिकी के प्रसार को सक्षम करके हमारी दुनिया को बदल दिया है।
- प्रमुख अनुप्रयोग:
- पोर्टेबल इलेक्ट्रॉनिक्स: स्मार्टफोन, लैपटॉप, टैबलेट और पहनने योग्य उपकरणों को सशक्त बनाना।
- परिवहन: व्यक्तिगत और सार्वजनिक परिवहन दोनों के लिये इलेक्ट्रिक वाहनों (EV) का संचालन तथा जीवाश्म ईंधन पर निर्भरता को कम करना।
- नवीकरणीय ऊर्जा भंडारण: सौर पैनलों और पवन टर्बाइनों द्वारा उत्पन्न ऊर्जा को बाद में उपयोग के लिये संग्रहीत करना।
- दूरस्थ क्षेत्रों के लिये बिजली: दूरस्थ या ऑफ-ग्रिड स्थानों पर बिजली प्रदान करना जहाँ पारंपरिक बिजली स्रोत अनुपलब्ध या अविश्वसनीय हैं।
- इलेक्ट्रिक बैटरी एक ऐसा उपकरण है जो रासायनिक ऊर्जा को संग्रहीत करता है और इसे बिजली में परिवर्तित करता है।
- बैटरियों के प्रमुख प्रकार:
- सॉलिड-स्टेट बैटरी: यह एक ऐसी बैटरी है जो लिक्विड या पॉलिमर जेल इलेक्ट्रोलाइट के बजाय सॉलिड इलेक्ट्रोड और सॉलिड इलेक्ट्रोलाइट का उपयोग करती है।
- सॉलिड-स्टेट बैटरियों का उपयोग विभिन्न उपकरणों में किया जाता है, जिनमें शामिल हैं: पेसमेकर, रेडियो फ्रीक्वेंसी आइडेंटिफिकेशन (RFID) और पहनने योग्य डिवाइस।
- निकेल-कैडमियम बैटरी (Ni-Cd): इनका उपयोग ताररहित इलेक्ट्रॉनिक उपकरणों, ड्रिल, कैमकोर्डर और अन्य छोटे बैटरी चालित उपकरणों के लिये किया जाता है, जिनके लिये समान पावर डिस्चार्ज की आवश्यकता होती है।
- क्षारीय बैटरी: यह एक प्रकार की प्राथमिक बैटरी है जो इलेक्ट्रोड के रूप में जिंक और मैंगनीज़ डाइऑक्साइड का उपयोग करती है।
- इसका उपयोग उन अनुप्रयोगों के लिये किया जाता है जिनके लिये कम लागत और विश्वसनीय विद्युत की आवश्यकता होती है, जैसे- फ्लैशलाइट, खिलौने, रेडियो और रिमोट कंट्रोल।
- लिथियम-आयन बैटरी: ली-आयन बैटरी के अभूतपूर्व सिद्धांतों ने इसके डेवलपर्स को वर्ष 2019 में रसायन विज्ञान में नोबेल पुरस्कार दिलाया, जो 20वीं और 21वीं सदी में इसके गहरे प्रभाव को रेखांकित करता है।
- ली-आयन बैटरियाँ बहुमुखी हैं, जो फोन और लैपटॉप जैसे पोर्टेबल उपकरणों को ऊर्जा प्रदान करने के साथ-साथ कारों और बाइक जैसे इलेक्ट्रिक वाहनों के लिये भी उपयोगी हैं।
- सॉलिड-स्टेट बैटरी: यह एक ऐसी बैटरी है जो लिक्विड या पॉलिमर जेल इलेक्ट्रोलाइट के बजाय सॉलिड इलेक्ट्रोड और सॉलिड इलेक्ट्रोलाइट का उपयोग करती है।
- विद्युत रासायनिक सेल:
- इलेक्ट्रोकेमिकल सेल ऐसे उपकरण हैं जो रासायनिक ऊर्जा को विद्युत ऊर्जा में परिवर्तित कर सकते हैं, या इसके विपरीत प्रतिक्रिया करते हैं।
- वे रासायनिक प्रतिक्रियाओं के माध्यम से विद्युत प्रवाह उत्पन्न कर सकते हैं या रासायनिक प्रतिक्रियाओं को सुविधाजनक बनाने के लिये विद्युत ऊर्जा का उपयोग कर सकते हैं।
- इलेक्ट्रोकेमिकल सेल, जैसे वोल्टाइक या गैल्वेनिक सेल, रेडॉक्स प्रतिक्रियाओं के माध्यम से संचालित होते हैं, जिसमें ऑक्सीकरण के दौरान इलेक्ट्रॉन मुक्त होते हैं और कमी के दौरान उपयोग किये जाते हैं।
- एक मानक सेल में विशिष्ट इलेक्ट्रोलाइट्स में डूबे धातु इलेक्ट्रोड को समायोजित करने वाले दो खंड होते हैं।
- इलेक्ट्रोड अर्थात् एनोड और कैथोड, विद्युत संचालन करते हैं।
- एनोड में जहाँ ऑक्सीकरण होता है, कैथोड, में अपचयन होता है, सेल के मूलभूत घटक बनाते हैं।
- एक मानक सेल में विशिष्ट इलेक्ट्रोलाइट्स में डूबे धातु इलेक्ट्रोड को समायोजित करने वाले दो खंड होते हैं।
- इलेक्ट्रॉन एक बाहरी सर्किट के माध्यम से नकारात्मक रूप से चार्ज किये गए एनोड से सकारात्मक रूप से चार्ज किये गए कैथोड में प्रवाहित होते हैं, जो विभिन्न प्रकार के उपयोगों के लिये ऊर्जा प्रदान करते हैं।
- इन हिस्सों को जोड़ने वाला एक तार और एक लवण सेतु है, जो उनके बीच आयनों की आवाजाही को सुविधाजनक बनाता है।
- इलेक्ट्रॉनों द्वारा ली गई ऊर्जा स्रोत वोल्टेज को निर्देशित करती है, जिससे सर्किट के भीतर इलेक्ट्रॉन प्रवाह नियंत्रित होता है।
- आदर्श परिस्थितियों में स्रोत वोल्टेज टर्मिनल वोल्टेज के बराबर होता है, जो एक कुशल विद्युत आपूर्ति सुनिश्चित करता है।
- सेल डिज़ाइन और सामग्रियों में प्रगति, निकल-कैडमियम, ज़िंक-कॉपर तथा आधुनिक लिथियम-आयन सेल में देखी गई, जो बढ़े हुए वोल्टेज एवं बढ़ी हुई दक्षता को दर्शाती है।
- इलेक्ट्रोकेमिकल सेल ऐसे उपकरण हैं जो रासायनिक ऊर्जा को विद्युत ऊर्जा में परिवर्तित कर सकते हैं, या इसके विपरीत प्रतिक्रिया करते हैं।
- संबंधित चुनौतियाँ:
- इलेक्ट्रोकेमिकल सेल की दक्षता को प्रभावित करने वाली प्रमुख चुनौतियों में से एक ‘जंग’ है। उदाहरण के लिये उच्च आर्द्रता वाले वातावरण में इलेक्ट्रोड जल की बूंँदों को इकट्ठा कर सकते हैं।
- यदि वायुमंडलीय कार्बन डाइऑक्साइड का स्तर ऊँचा हो जाता है, तो जल और गैस के संयोजन से कार्बोनिक एसिड का निर्माण होता है, जिससे इलेक्ट्रोड सतहों पर जंग लग जाती है।
- एक अन्य समस्या गैल्वेनिक संक्षारण से उत्पन्न होती है, जहाँ एक सेल के भीतर इलेक्ट्रोड में से एक अपनी उच्च प्रतिक्रियाशीलता के कारण इलेक्ट्रोलाइट में तेज़ी से खराब हो जाता है।
- उदाहरण के लिये कार्बन-ज़िंक बैटरी में बैटरी के उपयोग के दौरान जिंक इलेक्ट्रोड अधिक तेज़ी से नष्ट हो जाता है।
- इलेक्ट्रोकेमिकल सेल की दक्षता को प्रभावित करने वाली प्रमुख चुनौतियों में से एक ‘जंग’ है। उदाहरण के लिये उच्च आर्द्रता वाले वातावरण में इलेक्ट्रोड जल की बूंँदों को इकट्ठा कर सकते हैं।
बैटरियों का विकासपरक प्रक्षेप पथ क्या है?
- गैलवानी का प्रयोग (1780):
- लुइगी गैलवानी के धातुओं तथा मेंढक के पैरों से जुड़े प्रयोग से विद्युत ऊर्जा एवं मांसपेशियों की गति के बीच एक अनोखे संबंध का पता चला, जिसने भविष्य में बैटरी के विकास के लिये आधार तैयार किया।
- वोल्टाइक पाइल (1800):
- एलेसेंड्रो वोल्टा के वोल्टाइक पाइल ने धातु प्लेटों तथा इलेक्ट्रोलाइट्स का उपयोग करके एक स्थिर धारा उत्पन्न की जो एक महत्त्वपूर्ण कदम था।
- हालाँकि इसकी कार्यात्मकता एक रहस्य बनी रही।
- एलेसेंड्रो वोल्टा के वोल्टाइक पाइल ने धातु प्लेटों तथा इलेक्ट्रोलाइट्स का उपयोग करके एक स्थिर धारा उत्पन्न की जो एक महत्त्वपूर्ण कदम था।
- फैराडे की अंतर्दृष्टि (19वीं सदी की शुरुआत):
- माइकल फैराडे के अभूतपूर्व कार्य ने कोशिकाओं की व्यावहारिकता को समझा तथा एनोड, कैथोड और इलेक्ट्रोलाइट जैसे घटकों की भूमिकाओं का खुलासा किया।
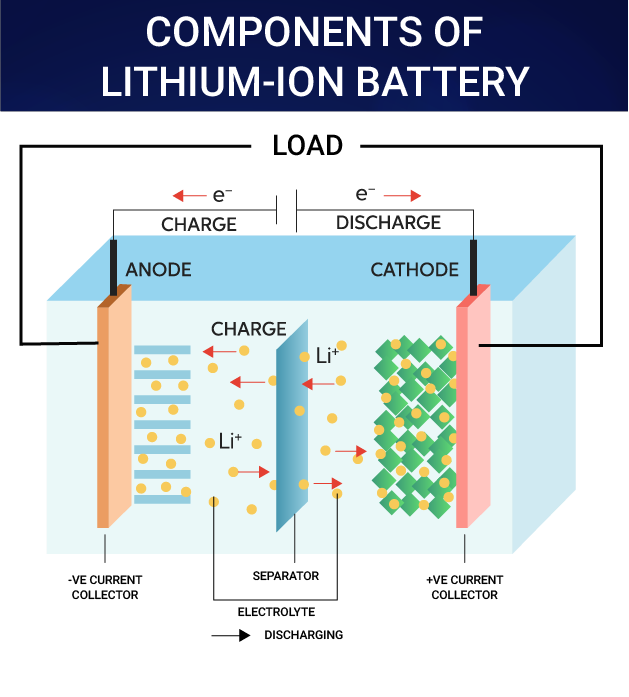
- लिथियम-आयन बैटरी: यह बैटरी वोल्टाइक तथा इलेक्ट्रोलाइटिक सेल दोनों के रूप में कार्य करती है, जो रासायनिक ऊर्जा को विद्युत ऊर्जा में परिवर्तित करने में सक्षम है तथा इसके विपरीत रिचार्जिंग को सक्षम बनाती है।
- लिथियम-आयन कोशिकाओं में लिथियम धातु ऑक्साइड तथा ग्रेफाइट क्रमशः कैथोड और एनोड के रूप में कार्य करते हैं, एक अर्द्ध-ठोस पॉलिमर जेल इलेक्ट्रोलाइट उन्हें अलग करता है।
- इंटरकैलेशन प्रक्रिया चार्ज एवं डिस्चार्ज चरणों को सक्षम बनाती है।
नोट: वर्ष 2019 के लिये रसायन विज्ञान में नोबेल पुरस्कार जॉन बी.गुडइनफ, एम. स्टेनली व्हिटिंगम तथा अकीरा योशिनो को लिथियम-आयन बैटरी के विकास में उनके योगदान के लिये प्रदान किया गया था।
UPSC सिविल सेवा परीक्षा, विगत वर्ष के प्रश्नप्रिलिम्स:प्रश्न. निम्नलिखित में से धातुओं का कौन-सा युग्म क्रमशः सबसे हल्की और सबसे भारी धातु का वर्णन करता है? (2008) (a) लिथियम और पारा उत्तर: (b) |